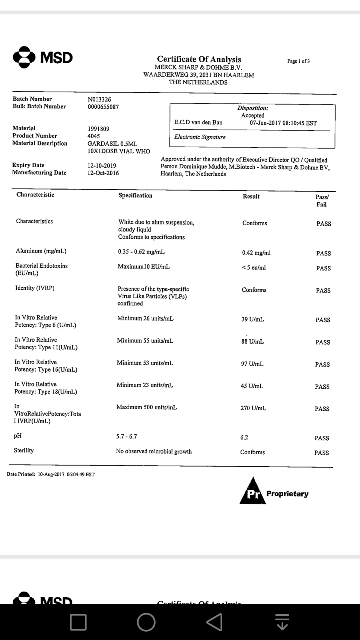
Գարդասիլ պատվաստանյութը Հայաստան ներկրվելուց առաջ լաբորատոր փորձաքննություն է անցել Նիդեռլանդներում
Հայաստան ներկրված մարդու պապիլոմավիրուսային վարակի դեմ գարդասիլ պատվաստանյութն արտադրվել է ամերիկյան Մերկ ընկերության կողմից 2016 թվականի հոկտեմբերի 12-ին՝ երեք տարի պիտանիության ժամկետով։ Պատվաստանյութի ամբողջ խմբաքանակը մինչև Հայաստան ներկրվելը փաստաթղթային և լաբորատոր փորձաքննություն է անցել Նիդեռլանդներում։ Եվրոպական այս երկրում ոլորտը կանոնակարգող մարմնի՝ Հանրային առողջության և շրջակա միջավայրի ազգային ինստիտուտի կողմից կատարվել է պատվաստանյութի արտադրության ամփոփիչ պրոտոկոլի փորձաքննություն։ 34.700 դեղաչափ պատվաստանյութի լաբորատոր հետազոտության արդյունքում տրամադրվել է համապատասխանության սերտիֆիկատ N 171337 (նկարում)։ Այս մասին տեղեկացրին ՀՀ առողջապահության նախարարությունից:
Սերտիֆիկատում նշվում է, որ N 013326 սերիայի պատվաստանյութը, որը ներկրվել է ՀՀ ՄԱԿ-ի մանկական հիմնադրամի միջոցով, համապատասխանում է ազգային և Առողջապահության համաշխարհային կազմակերպության ուղեցույցի Ա մասի պահանջներին, որոնք ապահովում են գենային ինժեներիայի ճանապարհով ստացված (ռեկոմբինանտ) վիրուսանման մասնիկներ պարունակող պատվաստանյութի անվտանգությունն ու արդյունավետությունը։ Սերտիֆիկատը նաև հավաստում է, որ պատվաստանյութի այս խմբաքանակն արտադրվել է կենսաբանական արտադրանքի հիմնական սկզբունքներին և պատշաճ արտադրական գործընթացին համահունչ։
Ներկայացվում են նաև լաբորատոր քննությունների արդյունքները։
Նշենք, որ ռեկոմբինանտ պատվաստանյութերը ներկայումս համարվում են ամենաանվտանգն ու արդյունավետը։ Հայաստանում 2000 թվականից ռեկոմբինանտ պատվաստանյութ կիրառվում է հեպատիտ Բ-ի կանխարգելման նպատակով մինչև մեկ տարեկան երեխաների շրջանում։